Aku tööpõhimõte
Kuidas seinakell, teleri kaugjuhtimispult või raadio teel juhitav laste mänguasi töötavad? Enamik inimesi vastab kõhklemata "patareidest" ja põhimõtteliselt on neil õigus. Kuid on ebatõenäoline, et keegi neist suudab öelda, kuidas kaasaskantav aku täpselt kolmekordistub, kuidas see töötab ja ilma milleta oleks kogu elektrivoolu edastamise protsess akust lõpptarbijale võimatu. Täitkem see tüütu teadmistelünk.
Aku tööpõhimõte
Tavalise AA-patarei tööpõhimõtte mõistmiseks peab teil olema üldine arusaam selle struktuurist. Niisiis, iga aku koosneb kolmest põhielemendist - anoodist, katoodist ja elektrolüüdist. Veelgi enam, viimastel võib olla peaaegu igasugune agregatsiooni olek: soolalahusesse asetatud katood ja anood on põhimõtteliselt samuti "aku", ainult tavainimese jaoks ebatavalisel kujul.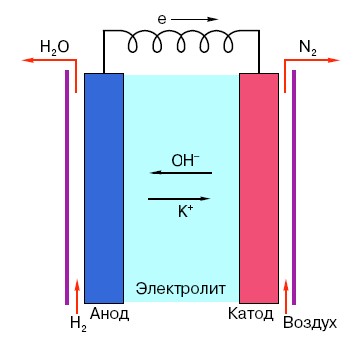
Huvitav! Alessandro Volta leiutatud nn "voltaic kolonn" sisaldas samuti kõiki elektrivoolu tootmiseks vajalikke elemente. See koosnes üksteise peale laotud tsink- ja vaskplaatidest, mille vahele asetati “kihina” happega immutatud riie.
Anood sellistes süsteemides on peamine elektronide allikas, mis, nagu teame koolifüüsika kursusest, on negatiivse laenguga.Negatiivselt laetud osakesed tõmbavad positiivseid osakesi ja sel juhul toimib katoodi pind "plussina".
Kuid sellest ei piisa elektrivoolu tekkeks, sest elektronid vajavad ka omamoodi "kiirteed" - keskkonda, mis toetaks katoodi ja anoodi koostoimet. Just siin ilmub "lavale" elektrolüüt - sool, leelis või hape, mis on võimeline voolu juhtima.
Vaatame tööpõhimõtet konkreetse näite abil: seal on aku, mille pinge on 18 volti. Pinge selles olevate elektroodide vahel on stabiilne, kuni see on võrku ühendatud. Niipea kui ilmub tarbija (näiteks tavaline lambipirn), hakkab pinge järk-järgult langema, vool hakkab voolama "negatiivselt" elektroodilt "positiivsele" ja elektrolüüdis toimub keemiline reaktsioon, mille eesmärk on elektroodide vahelise potentsiaalide erinevuse säilitamine.
Viide. Mida rohkem energiat tarbija vajab, seda intensiivsem on reaktsioon aku sees ja seda kiiremini see ebaõnnestub.
Kuidas laetav aku töötab, mille poolest see tavalisest erineb
Niisiis, oleme vaadanud klassikalisi "sõrme" ja "väikese sõrme" akusid ja teame, et enamiku nende kasutusiga on rangelt piiratud (ükskõik, mida kuulsad tootjad räägivad). Kuidas on aga lood nn patareidega – patarei-tüüpi patareidega, mis ei suuda reaktsiooniprotsessis mitte ainult energiat tarbida, vaid ka koguda seda ja säilitada seda pikka aega?
Aku tööpõhimõtte mõistmiseks on vaja pöörduda keemia poole. Võtame näiteks... Tavaline söetuli.Ükskõik kui ilus ja põnev leek välja ei näeks, teab iga seda jälgiv keemik, et see protsess on lihtsalt kütuse pikaajaline oksüdatsioonireaktsioon. Põlev kivisüsi interakteerub hapnikuga ja selle reaktsiooni tulemusena saame:
- süsinikdioksiid;
- valgus;
- soe.
Ja kui kaks viimast punkti on võimelised soojendama hinge ja keha, siis ei saa me süsihappegaasi kuidagi kasutada, sest see on reaktsiooni kõrvalsaadus, mis on tegelikult selle jäätmed. Oksüdatsioonireaktsioon peatub, kui lähteelemendid: hapnik ja kivisüsi otsa saavad. Reaktsiooni peatamine akus toimub täpselt samamoodi, kui lähteained on täielikult otsas ja järele jäävad vaid “jäätmed”.
Akus toimub kõik veidi teisiti. Fakt on see, et selles toimuv reaktsioon kuulub pöörduva kategooriasse, see tähendab, et teatud tingimustel saab seda "pöörata", tagastades kõik ained nende algsesse olekusse. See on võimalus, et akus võib tekkida pöörduv reaktsioon, mis võimaldab seda laadida.
Võrku ühendatud akus toimub reaktsioon vastupidises suunas ja vool liigub "plussist" "miinusesse", mitte vastupidi. Selle tulemusena moodustub reaktsioonisaadus lähteained ja aku omanik saab kaasaskantavas vormingus saadaoleva "taastatud" energia. See on kõik!





